Belajar Kimia-Metode dialisis digunakan untuk memisahkan molekul-molekul yang besar dari molekul molekul yang kecil. Suatu membran yang semipermeabel membiarkan molekul-molekul kecil melaluinya, tetapi mencegah molekul-molekul yang besar melalui membran tersebut. Dalam suatu percobaan, campuran dari molekul-molekul yang besar dan kecil ditempatkan dalam kantung dialisis yang dicelupkan ke dalam pelarut berair dalam jumlah lebih banyak. Molekul-molekul yang berukuran kecil akan keluar melalui membran semipermeabel ke dalam pelarut atau bufer, sampai tercapai kesetimbangan antara cairan di dalam dan di luar kantung seperti pada gambar berikut ini.
 |
| Dialisis Campuran yang mengandung molekul besar dan kecil |
Campuran dari molekul ini dapat dibebaskan dari molekul kecil dengan melakukan dialisis terhadap air yang mengalir, atau dengan berulang kali mengganti pelarutnya.
Kecepatan dialisis tergantung pada beberapa faktor yang akan dibahas secara singkat seperti berikut ini.
Membran Saat ini, selofan merupakan bahan yang umum dipakai sebagai membran dalam proses dialisis. Selofan ini berupa tabung yang dibuat oleh Visking Division dari Union Carbide.
Membran selofan mengandung sejumlah kecil senyawa-senyawa sulfur, ion logam. dan beberapa enzim, oleh karena itu dianjurkan agar setiap tabung dididihkan selama 30 menit dalam alkali EDTA (Na,CO, 10 g/L, EDTA 1 mmol/L) untuk mencegah hilangnya aktivitas molekul-molekul yang dialisis. Setelah didinginkan, tabung-tabung tersebut lalu dicuci dengan aquades, kemudian salah satu ujungnya diikat dengan benang rami yang dapat dilihat pada gambar diatas. Tabung yang berbentuk kantung diisi dengan bahan yang akan dialisis, dan ujung yang satunya diikat lagi. Dialisis paling baik dilakukan dengan tabung yang baru saja disiapkan, karena bila sudah basah, kantung akan peka terhadap serangan mikroorganisme. Jika harus disimpan, maka kantung selofan harus disimpan dalam larutan yang telah dibubuhi sedikit asam benzoat sebagai pengawet.
Batas permeabilitas dari tabung Visking yang telah dipersiapkan, tergantung pada ukuran dan perlakuan awal. Membran dapat dipakai jika bersifat permeabel bagi senyawa-senyawa yang berat molekulnya di bawah 30.000 dan bila dialisisnya dilakukan dari malam sampai pagi hari. Pada prakteknya, tidak ada ketentuan yang pasti bahwa molekul yang lebih besar dapat berdifusi melalui membran tersebut bila waktu dialisisnya diperpanjang. Terdapat sejumlah bahan-bahan komersial dengan laju alir yang tinggi dan batas-batas yang cukup jelas untuk permeabilitas yang dapat digunakan dalam pemisahan-pemisahan yang lebih halus.
Pelarut Pada umumnya, kecepatan dialisis akan maksimal jika menggunakan pelarut aquades, meskipun kecepatan dialisis suatu larutan ditentukan oleh pH dan kekuatan ionisasi zat terlarut yang diperlukan untuk menstabilkan molekul-molekul yang didialisis Selama dialisis terjadi, proses osmosis menyebabkan masuknya air ke dalam kantung dialisis, sehingga kantung dialisis selalu terisi penuh sebelumnya untuk menghindari terjadinya pengenceran yang berlebih dari molekul-molekul yang ada di kantung dialisis. Jika larutan pekat dari suatu senyawa yang inert dengan berat molekul yang tinggi digunakan sebagai pelarut pengganti, maka air dalam kantung dialisis akan keluar karena terjadinya osmosis. Pada kondisi ini, pelarut yang banyaknya kira-kira 200 mL dapat keluar dari kantung dialisis dalam waktu semalam, sehingga yang tinggal hanya beberapa ml di dalam kantung. Dalam hal ini terjadi pemekatan senyawa di dalam kantung
Sifat-sifat fisik Kecepatan dialisis juga tergantung pada suhu, sehingga semakin tinggi suhu di sekitarnya, maka semakin tinggi pula kecepatan dialisisnya. Jika suhu ditingkatkan, maka viskositas dari pelarut berkurang, sehingga kecepatan dialisis meningkat. Sebaliknya, banyak makromolekul yang sensitif terhadap suhu.
jadi dialisis terhadap protein dan sebagainya selalu dilakukan pada suhu yang lebih rendah (dalam kondisi dingin atau di dalam ruangan berpendingin).
Pemisahan antara molekul-molekul yang besar dan kecil dapat pula dipengaruhi oleh tekanan atau perubahan yang terjadi pada membran. Hal ini dapat dilakukan secara mudah dengan menempatkan kantung dialisis dalam suatu ruang vakum Air dan molekul-molekul yang kecil akan keluar dari kantung dialisis menembus membran, membentuk suatu ultrafiltrat, sedangkan molekul-molekul yang besar akan tetap tinggal di dalam kantung dalam keadaan terkonsentrasi. Proses seperti ini dikenal dengan nama ultrafiltrasi
Kesetimbangan membran Donnan Bila suatu larutan makromolekul seperti protein dipisahkan dari suatu larutan garam dengan membran semipermeabel, maka protein yang bermuatan listrik tidak dapat menembus membran tersebut, akan tetapi ion-ionnya dengan muatan yang berlawanan cenderung dapat menembus membran. Hal ini mengakibatkan suatu distribusi yang tidak merata dari ion-ion dan akan terjadi suatu perbedaan potensial listrik melalui membran
Efek Donnan merupakan dasar dari fenomena listrik dalam fisiologi. Akan tetapi, efek ini tidak mudah diamati (sulit terjadi) bila dialisisnya dilakukan dengan menggunakan aquades sebagai pelarutnya dan terjadi perubahan pH. Misalnya, apabila suatu larutan protein yang bermuatan negatif dalam larutan NaCL (salin) didialisis dalam aquades yang ada di luar kantung dialisis), maka protein ini tidak dapat menembus dinding kantung, akan tetapi ion-ion yang bermuatan positif (Na+) bebas untuk menembus dinding kantung dialisis. Hal ini akan mengakibatkan kelebihan kation di seluruh medium, dan muatan elektron medium akan dinetralisasi, air terdisosiasi, dan ion-ion hidrogen bermigrasi masuk ke dalam kantung dialisis. Dengan demikian, pH di dalam protein kompartemen (medium di dalam kantung yang mengandung protein) mengalami penurunan, sedangkan yang berada di luar kantung mengalami kenaikan seperti pada gambar berikut:
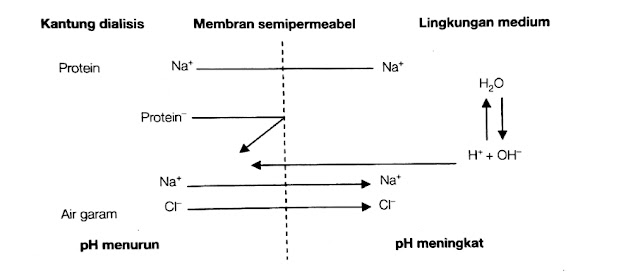 |
| Efek Donnan terlihat ketika larutan protein berada dalam larutan garam yang akan didialisis berlawanan dengan aquades |
Apabila protein di dalam kantung dialisis bermuatan positif, maka perubahan pH yang terjadi adalah sebaliknya. Perubahan-perubahan pH seperti ini tidak dikehendaki, dan mengakibatkan presipitasi atau denaturasi protein.
Distribusi yang tidak merata dari ion-ion ini tidak dikehendaki, dan untuk mengurangi efek Donnan ini, dialisis sering kali dilakukan terhadap larutan-larutan dengan konsentrasi garam yang kadarnya sedang (lebih kecil dari 0,1 mol/L). Skema efek Donnan ketika larutan protein dalam larutan garam NaCl dialisis dengan aquades ditunjukkan pada Gambar diatas.
Sumber: Teknik Penelitian Biokimia Maria Bintang
_page-0025.jpg)




