|
| Ayo Belajar Menuliskan Mekanisme Reaksi |
Agar bisa memahami
dengan mudah kimia organik dan khususnya organik sintesis maka harus dipahami
pendekatan umum yang dilakukan dalam menuliskan mekanisme reaksi sebagai
berikut:
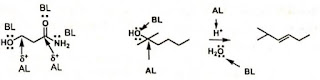
1. Gambarkan jumlah
pasangan elektron non-ikatan pada heteroatom (O, N,S dll) pada penulisan struktur
kimia, sehingga dengan mudah dapat diketahui pusat atau atom yang dapat
bertindak sebagai asam Lewis dan basa Lewis
2. Tentukan pereaksi
yang berfungsi sebagai basa Lewis (BL) dan Asam
Lewis (AL)
3 Gunakan Anak panah
melengkung untuk mengindikasikan pergerakan
elektron dari atom
donor (pasangan elektron non-ikatan atau ikatan Pi)
Ke atom penerima yang
kekurangan elektron.
4. Jika terdapat
lebih dari satu gugus fungsi yang dapat menyumbangkan pasangan elektron
non-Ikatannya, maka periksa gugus fungsi mana yang pertama melakukan reaksi.
Sebagai pertimbangan dalam menentukan prioritas reaksi adalah kestabilan dari
karbokation permulaan. Karbokation yang paling stabil adalah yang paling mudah
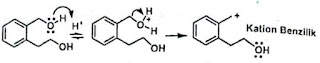
dibentuk. Sebagai gambaran
dapat dilihat dari
contoh berikut: Karbokation benzilik lebih mudah terbentuk dari karbokation
primer
5 Kebanyakan
mekanisme khususnya yang melibatkan penataan ulang bisa terjadi dalam beberapa
tahap Reaksi dari setiap tahap kebanyakan adalah reaksi antara Basa Lewis
dengan Asam Lewis baik antar molekul atau intermolekul. Kekuatan penggerak pada
tahap ini adalah tingkat
kestabilan
karbokation Contoh karbokation yang kurang stabil akan melakukan penataan ulang
membentuk karbokation yang lebih stabil.
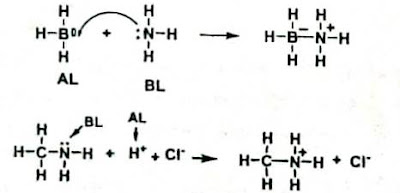
Secara umum reaksi
antara asam Lewis dan Basa Lewis dapat digambarkan sebagai berikut
Bagaimana reaksi
organik digambarkan secara demikian, maka produk reaksi bisa dengan mudah
diprediksi tanpa memerlukan daya ingat yang kuat Sebagai Ilustrasi dapat
dilihat pada contoh berikut: